
答:input是阳性对照。免疫共沉淀实验中,会直接取细胞裂解液进行WB,用于验证细胞裂解液中确实存在目的蛋白,即阳性对照。
答:最好选择两个不同种源的抗体。选择同一种源的抗体的问题在于:在WB之前进行的蛋白变性这一步,由于加样缓冲液中含有巯基乙醇,巯基乙醇会把抗体的重链和轻链之间的二硫键破坏,从而使的抗体变成重链分子55KD和轻链分子25KD。假设你IP的抗体是兔抗的,目的蛋白进行WB的抗体也是兔抗的,而且目的蛋白的分子量为55KD,可以想象,55KD的位置除了你的目的蛋白以外,还有IP抗体的重链IgG。由于IP的抗体用量非常大(1ug),就导致55KD处的信号会非常强。如果你用抗兔的二抗进行显色,那么55KD处的ip抗体的重链和你的目的蛋白会重叠在一起,无法分辨。
然而这个时候如果你的目的蛋白进行WB的抗体不是兔抗的,比如小鼠抗的,那么就需要用抗小鼠的二抗进行显色,而抗小鼠的二抗是无法跟兔抗的IP抗体发生反应的。因此55KD位置的IP抗体的重链IgG就无法显色,发生反应的就是你的目的蛋白了。
答:若抗体浓度高,则降低抗体浓度;若抗体特异性不好,则换抗体;若PCR污染,则重新配置缓冲溶液。
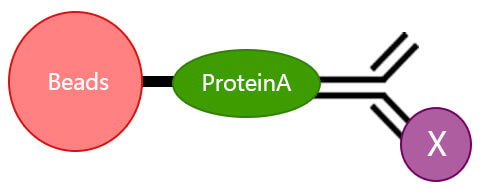
答:ProteinA/G能特异性地结合到免疫球蛋白的FC片段,因此能和抗体结合,而抗体与目标蛋白结合,目标蛋白和相互作用的蛋白结合。
答:排出污染的可能性,例如检测一个兔子细胞的某种蛋白质,若没有设置LgG的对照,而操作中有非特异性蛋白质,又和设计的抗体有作用,就会出现阳性的结果。如果做了阴性对照,也就是lgG对照,对照没有出现阳性就说明没有非特异性的蛋白,对照出现阳性,说明抗体有非特异结合的可能,需要重新开始实验。
答:用兔的lgG做对照;用抗Fab和Fc抗体特异性封闭轻链和重链;在WB二抗上着手,这种二抗针对的是轻重链间的二硫键,若跑SDS胶,最后显影是检测不到重链和轻链的。
答:裂解液中的去垢剂浓度太高或配方过于剧烈:此时降低去垢剂浓度或更换去垢剂种类;
受蛋白的亚细胞定位影响:应重新选择裂解液配方来释放目的蛋白;
蛋白与蛋白之间的相互作用太弱或不太稳定:应选择亲和力更高的抗体以捕获更多的目的蛋白,从而捕获更多的相互作用蛋白;过表达提高目的蛋白的含量:选择目的蛋白或相互作用蛋白含量高的样品进行免疫共沉淀实验。
 免疫沉淀
免疫沉淀免疫沉淀(immunoprecipitation)是指利用抗体可与抗原特异性结合的特性,将抗原(常为靶蛋白)从混合体系沉淀下来,初步分离靶蛋白的一种方法。
免疫共沉淀(coimmunoprecipitation)是一种在体外探测两个蛋白分子间是否存在特异性相互作用的一种方法。其原理非常简单,如果两个蛋白在体外体系能够发生特异性相互作用的话,那么当用一种蛋白的抗体进行免疫沉淀时,另一个蛋白也会被同时沉淀下来。与酵母双杂交技术不同,免疫共沉淀技术所利用的是抗原和抗体间的免疫反应,是一种基于体外非细胞的环境中研究蛋白质与蛋白质的相互作用的方法。
免疫共沉淀与免疫沉淀技术所使用的原理与方法大致相似,所不同的是,在免疫共沉淀中,对靶蛋白的结合与沉淀由另一个与之发生相互作用的蛋白替代。在免疫共沉淀或免疫沉淀的基础上,通过进一步与其它技术的结合,如聚丙烯酰胺凝胶电泳,还可进一步对靶蛋白的的分子量等特性进行鉴定。
答:非特异蛋白结合,处理方法:在无血清培养液中裂解细胞; 在免疫沉淀前用protein (G/A)珠子预洗免疫沉淀后增加漂洗次数和严谨度(高盐或去垢剂),裂解液严谨度太低,处理方法:改用高严谨度裂解液,实验仪器或液体被污染,处理方法:使用洁净的仪器或液体转移膜上的非特异吸附,处理方法:戴手套, 用镊子夹取, 不要接触膜转移面。
样品被蛋白酶降解,处理方法:添加蛋白酶抑制剂(protease inhibitor);所有操作保持4℃以下冰上操作并防止冻融。
抗体浓度太低,处理方法:调整IP和/或IB抗体浓度, 必要时设立浓度梯度,摸索最佳浓度;
抗体亲合力太低,处理方法:选用适合于IP和/或IB的相应抗体;
IP抗体未与agarose珠子结合,处理方法:选用适合于IP的相应珠子, 正确保存防止变质或干燥;
Tag未暴露在融合蛋白构象的表面,处理方法:改变tag融合表达部位;
裂解液严谨度太高,处理方法:改用低严谨度裂解液。
答:一般有三种反应顺序:1.样本+抗体先反应,然后加磁珠;2.抗体+磁珠先反应,然后放入样本中;3.样本+抗体+磁珠同时反应。推荐使用第一种和第二种,差别不大。不推荐用第三种,第三种方式虽然可以减少反应时间,但有实验表明同时加入三个组分的方式会使最终的结果变差。

南京德泰生物工程有限公司 Nanjing Detai Bioengineering Co.,Ltd. ©2025 All Rights Reserved